Періодична система хімічних елементів або таблиця Менделєєва — це винахід, що став революційним для науки та людства. Вшанування періодичної таблиці відбувається щороку 7 лютого у День періодичної системи хімічних елементів. Підготували для вас цікаві факти про періодичну систему хімічних елементів.
Періодичний закон є одним з найважливіших відкриттів у хімії. Він допоміг не лише класифікувати елементи, а й передбачити нові. Сучасна таблиця заснована на принципах квантової механіки та досі залишається ключовим інструментом у науці. Менделєєвська спадщина продовжує допомагати хімікам, фізикам і матеріалознавцям у всьому світі.
Історія періодичного закону
Розвиток аналітичної хімії на початку XIX століття привів до швидкого накопичення знань про хімічні та фізичні властивості елементів і сполук. Потреба у класифікації стала очевидною, адже без систематизації було складно передавати знання від одного покоління хіміків до іншого. Розглянемо хронологію винайдення періодичного закону.
У 1817 році Йоганн Вольфганг Деберейнер помітив, що атомна маса стронцію знаходиться між масами кальцію та барію. Надалі він виявив аналогічні “тріади” серед інших елементів, таких як галогени (хлор, бром, йод) та лужні метали (літій, натрій, калій). Його ідеї були розвинені іншими хіміками, такими як Жан-Батист Дюма, Леопольд Гмелін і Макс фон Петтенкофер.
У 1864 році Джон Ньюлендс запропонував класифікацію елементів за зростанням їхньої атомної маси. Він виявив, що кожен восьмий елемент має схожі властивості, і назвав це “законом октав” за аналогією з музичною шкалою. Однак ця модель була далека від досконалості.
У 1869 році Дмитро Менделєєв, провівши масштабний аналіз властивостей елементів, сформулював періодичний закон:
“Елементи, розташовані в порядку зростання атомної маси, проявляють періодичну зміну властивостей”.
Незалежно від нього, Лотар Мейєр дійшов подібного висновку.
Перша періодична таблиця
Менделєєвська таблиця 1869 року містила 17 стовпців і два майже завершені періоди елементів – від калію до брому та від рубідію до йоду. У 1871 році Менделєєв переглянув таблицю, правильно розташувавши 17 елементів. І найцікавіше: він також залишив пусті місця для ще не відкритих елементів, передбачивши їхні властивості. Згодом це дозволило передбачити існування скандію, галію і германію.
З відкриттям інертних газів, таких як гелій, неон, аргон, ксенон і радон, наприкінці XIX століття було введено нову “нульову” групу в періодичній таблиці. Наука – гнучка і мінлива. Після цього форма таблиці змінювалася, включаючи короткоперіодичну форму та інші варіанти.
Значення атомного номера
Спочатку порядок розташування елементів у таблиці визначався їхньою атомною масою, але лише в другому десятилітті XX століття було визнано, що основою впорядкування є атомний номер, який відповідає заряду ядра атома. Пізніші дослідження електронної будови атомів допомогли краще пояснити періодичний закон і розширити його значення.
Попри уточнення атомних мас, у деяких випадках елементи не вкладалися в логічну послідовність Менделєєва. Наприклад, калій мав меншу атомну масу, ніж аргон, але розташовувався після нього. Розв’язання цієї проблеми знайшли після відкриття структури атомного ядра.
- У 1910 році Ернест Резерфорд встановив, що заряд ядра пропорційний атомній масі.
- У 1913 році Генрі Мозлі, досліджуючи спектри рентгенівського випромінювання, підтвердив, що елементи мають унікальні атомні номери, які й визначають їх місце у періодичній таблиці. 1
Періодична система та квантова механіка
Розвиток квантової механіки у XX столітті значно розширив розуміння періодичного закону. Важливими етапами стали:
- Відкриття принципу виключення Паулі (1925 рік), який пояснив заповнення електронних оболонок.
- Розробка хвильової механіки Шредінгером і Гейзенбергом.
- Формулювання теорії валентності Гілбертом Льюїсом.
Цікаві факти про періодичну систему хімічних елементів
- Періодична таблиця зараз містить 118 елементів. Дев’яносто з них зустрічаються в природі, а решта є штучно створеними. Першим синтетичним елементом став технецій (Tc), який був отриманий у 1937 році.
- Водень (H) є першим елементом, а оганессон (Og) – останнім.
- Останніми названими елементами є 113, 115, 117 і 118. 28 листопада 2016 року IUPAC затвердила для них назви: ніхоній (Nh), московій (Mc), теннесин (Ts) і оганессон (Og).
- Найпоширенішим елементом у Всесвіті є водень (H), що становить приблизно 75% від усього спостережуваного космосу.
- Другим за поширеністю елементом є гелій (He). Разом водень і гелій складають понад 99% Всесвіту.
- Близько 75% періодичної таблиці складається з металів, серед яких лужні, лужноземельні, перехідні метали, лантаноїди та актиноїди.
-
Перша періодична таблиця була створена російським хіміком Дмитром Менделєєвим.
Дмитро Менделєєв представив свою таблицю хімічних елементів 6 березня 1869 року на засіданні Російського хімічного товариства. Він розташував елементи за зростанням їхньої атомної маси. - Цікаво, що до нього спроби систематизувати елементи вже здійснювалися. Наприклад, у 1864 році Лотар Меєр створив таблицю, що включала 28 елементів, згрупованих за їхніми властивостями.
- Для визначення маси 63 відомих на той час елементів вчені використовували електричні струми, що проходили через розчини. Полярність батарей спрямовувала атоми різних елементів у різні боки, після чого вони збиралися у відповідних контейнерах і зважувалися.
- Сучасна таблиця групує елементи за зростанням атомного номера, на відміну від таблиці Менделєєва, яка впорядковувала елементи за атомною масою.
- Періодична система хімічних елементів передбачила відкриття нових елементів. В оригінальній таблиці Менделєєва було кілька порожніх місць. Він припустив, що ці місця займуть ще не відкриті елементи, і навіть передбачив їхні хімічні властивості. Так він вгадав існування галію, скандію та германію задовго до їх відкриття. Але також періодична система хімічних елементів заперечувала існування деяких елементів. Попри свої успіхи, Менделєєв помилявся щодо деяких елементів. Наприклад, він заперечував існування аргону, відкритого у 1894 році, оскільки той не вписувався у його систему. Подібна ситуація була з гелієм, неоном, криптоном, ксеноном і радоном.
- Періодична таблиця постійно оновлюється. За періодичною таблицею стежить Міжнародний союз теоретичної та прикладної хімії (IUPAC). Останнє її оновлення було опубліковане у грудні 2018 року.
- Єдина літера, яка відсутня серед символів елементів у періодичній таблиці – J.
- Деякі елементи названі на честь відомих людей, місць чи міфології. Ейнштейній названий на честь Альберта Ейнштейна, а германій, америцій і галій – на честь місць їх відкриття. Уран назвали на честь планети Уран, а торій – на честь скандинавського бога Тора.
- Інші елементи отримали назви з грецької мови. Наприклад, аргон походить від грецького «Argos», що означає «лінивий» (через його інертність). А бром назвали на честь грецького слова «bromos», що означає «сморід», через його неприємний запах.
-
Любов Менделєєва до карткових ігор відобразилася на таблиці.
Менделєєв був великим шанувальником карткових ігор, тому для створення таблиці записував масу кожного елемента на окремій картці та впорядковував їх за принципом гри в пасьянс. Елементи з подібними властивостями формували «масть» і розташовувалися у стовпчиках. 2 - Елементи на протилежних кінцях таблиці можуть стабільно поєднуватися. Якщо розрізати сучасну періодичну таблицю, прибравши середні колонки, і скласти її вздовж елементів 4-ї групи, то «дотичні» елементи виявляться тими, що можуть стабільно утворювати сполуки.
- Вуглець – найважливіший елемент. Атоми вуглецю можуть формувати чотири ковалентні зв’язки, що дозволяє їм утворювати безліч різних молекул, включаючи кільця та решітки. Ця гнучкість робить вуглець ключовим елементом для життя.
- Ми складаємося приблизно на 20% з вуглецю, а більшість відомих сполук містять саме цей елемент. Він також є четвертим за поширеністю елементом у Всесвіті.
- Фізик Річард Фейнман припустив, що якщо 137-й елемент існуватиме, ми ніколи не зможемо його спостерігати. Причина в тому, що електрони цього елемента оберталися б зі швидкістю світла, що теоретично неможливо. 2
Читайте також: Містер Фейнман – видатний фізик та великий жартівник

Будова періодичної системи хімічних елементів
Періодична таблиця, на перший погляд, може здатися складною. Проте вона є впорядкованою системою всіх відомих елементів. Вони розташовані за зростанням атомного номера, що відповідає кількості протонів у ядрі атома.
Елементи впорядковані так, що ті, які мають подібні властивості, групуються разом. Періодична таблиця складається з вертикальних стовпців (груп) та горизонтальних рядів (періодів), що допомагає зрозуміти хімічні характеристики кожного елемента.
Періодична таблиця в хімії – це впорядкована система всіх хімічних елементів за зростанням їх атомного номера, тобто кількості протонів у ядрі атома. При такому впорядкуванні спостерігається закономірність, названа “періодичним законом”, згідно з яким елементи, що знаходяться в одному стовпці (групі), мають схожі властивості.
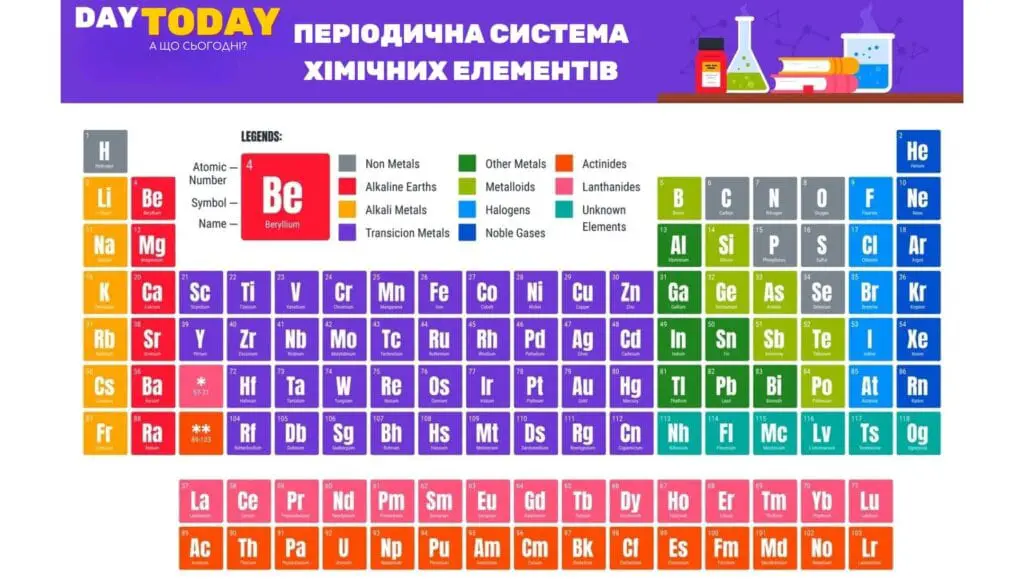
Періодична таблиця складається з горизонтальних рядів (періодів) і вертикальних стовпців (груп). У ній:
- Перший період містить два елементи (водень і гелій).
- Другий і третій – по вісім елементів.
- Четвертий і п’ятий – по 18 елементів.
- Шостий період містить 32 елементи, включаючи лантаноїди.
- Сьомий період також містить 32 елементи, включаючи актиноїди.
Групи елементів
Елементи згруповані за хімічними властивостями:
- Лужні метали (Група 1) – надзвичайно реактивні.
- Лужноземельні метали (Група 2) – мають схожі характеристики.
- Перехідні метали (Групи 3-12) – володіють змінною валентністю.
- Галогени (Група 17) – високореактивні неметали.
- Інертні гази (Група 18) – мають стабільну електронну конфігурацію.
Систематизація хімічних знань та лабораторних методів стала необхідною через швидке розширення знань у цій науці. Періодична таблиця допомагає зберігати й передавати хімічну інформацію від одного покоління хіміків до іншого. Хай вас надихають на навчання та наукові дослідження й винаходи цікаві факти про періодичну систему хімічних елементів!
Таким чином, початкове відкриття, зроблене Дмитром Менделєєвим у середині XIX століття, стало неоціненним внеском у розвиток хімії.
Cкільки елементів в періодичній системі?
Періодична таблиця зараз містить 118 елементів. Останніми названими елементами є 113, 115, 117 і 118. 28 листопада 2016 року IUPAC затвердила для них назви: ніхоній (Nh), московій (Mc), теннесин (Ts) і оганессон (Og).
Скільки елементів було у першій періодичній таблиці елементів?
Перша версія Періодичної системи хімічних елементів (1869 р.) Дмитра Менделєєва містила 63 хімічні елементи.
Читайте також: Математичні парадокси та софізми

Все найцікавіше за тиждень?
Щопʼятниці отримуйте найцікавіші статті за тиждень на ваш імейл.
Хоче сповіщення ЩОДНЯ? Тоді вам на ТГ-канал DAY TODAY (цікаве 🌍)












